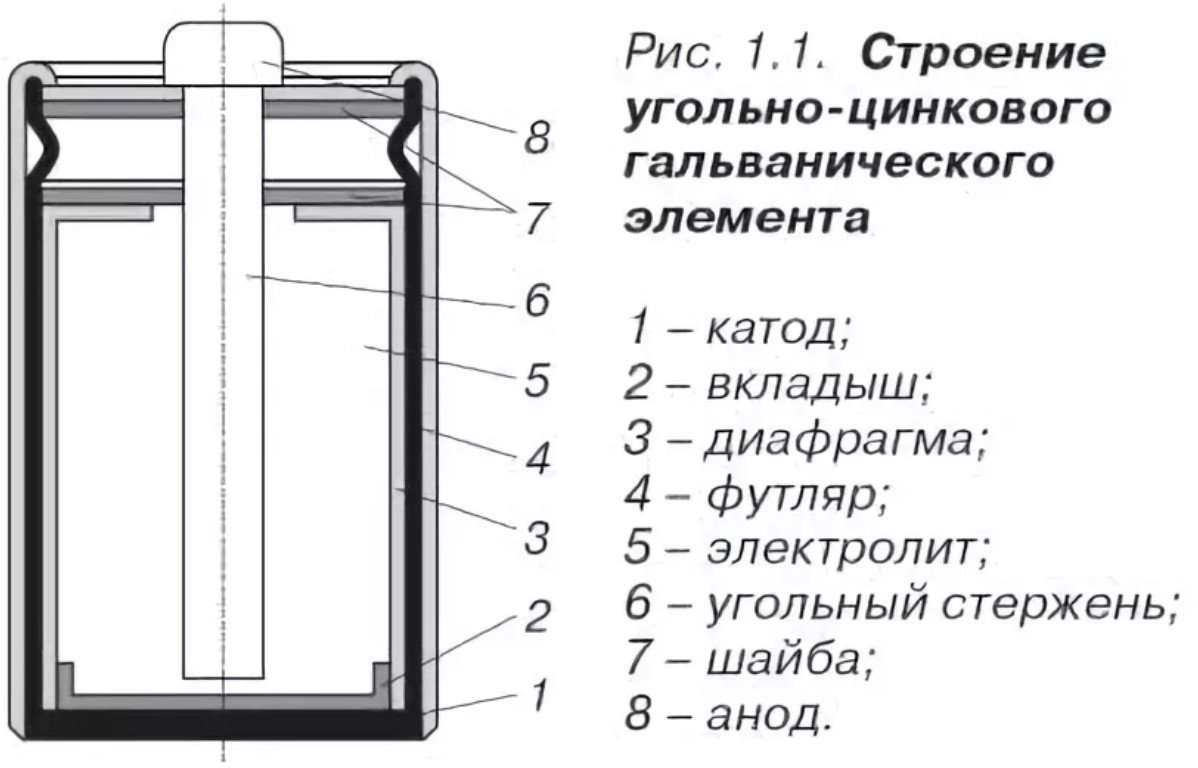
Ang malawakang paggamit ng maliliit na kagamitan sa bahay ng mga mamimili ay nangangailangan ng pangangailangan para sa mga pinagmumulan ng kuryente, o mga single-supply circuit. mga selulang galvaniko, karaniwang kilala bilang mga baterya. Una silang lumitaw noong 1800, salamat sa Italyanong pisiko na si Alessandro Volta. Nag-iiba-iba ang mga ito sa laki at hugis, boltahe, kapasidad, at uri ng baterya. Ang mga bateryang alkaline at saline ay malawakang ginagamit sa merkado ng maliliit na kagamitan at elektroniko.
Ano ang mga baterya ng asin?
Mga baterya ng asin — mga pinagmumulan ng kuryenteng nalilikha sa isang simpleng aparato sa pamamagitan ng isang kemikal na reaksyon. Minsan ay tinatawag itong mga bateryang carbon-zinc o mga bateryang carbon. Ang ganitong uri ng selula ay itinuturing na pinakamura, ngunit may mababang densidad ng enerhiya, kaya angkop ito para sa mga aparatong mababa ang lakas. Sa mga aparatong may mataas na konsumo ng kuryente o may katangiang pagtaas ng kuryente at temperatura ng karga, hindi ito nagtatagal at samakatuwid ay hindi ginagamit.
Pagtatalaga ng mga baterya ng asin
Ang pagtatalaga ng mga baterya ng asin ay tinatanggap ayon sa ilang mga pamantayan:
- Sistema ng klasipikasyon ng Amerika.
- Sistemang Pandaigdig (IEC).
- Pamantayang Interstate (GOST).
| Sistema ng klasipikasyon ng Amerika | Internasyonal na Klasipikasyon IEC | GOST | Sukat, milimetro | Kapasidad, mAh |
| Isang | R23 | 17x50 | ||
| AA | R6 | 316 | 14.5x50.5 | 1100 |
| AAA | R03 | 286 | 10.5x44.5 | 540 |
| C | R14 | 343 | 26.2x50 | 3800 |
| D | R20 | 373 | 34.2x61.5 | 8000 |
| F | R25 | 33x91 | ||
| 1/2AA | R14250 | 312 | 14.5x25 | 250 |
| R10 | R10 | 332 | 21.5x37.3 | 1800 |
Halimbawa, ang pagmamarka ng isang saline battery na R 6 ay nangangahulugang: bilog, silindriko, daliri, elementong uri ng asin, kabuuang sukat na 14.5x50.5, kapasidad1100 mAh. Ang karaniwang boltahe ay 1.5V. Ang "R" na disenyo (asin) sa etiketa ng baterya ay nagpapaiba sa mga saline na baterya mula sa iba pang mga uri ng baterya (alkaline o lithium).
Disenyo at komposisyon
Ang disenyo ng baterya ng asin ay medyo simple at binubuo ng:
- Katod - pareho ang kaso ng baterya ng asin ay ginawa gawa sa zinc, na may pinahusay na mga katangiang anti-corrosion at mataas na antas ng purification (minus).
- Ang anode ay isang agglomerate, ginawa sa pamamagitan ng pagpindot, pinapagbinhi ng electrolyte (kasama).
- Elektrolito: ammonium chloride o zinc chloride, na may dagdag na pampalapot (starch).
- Konduktor ng kasalukuyang carbon - tumatakbo sa gitna, ginagamot ng komposisyon ng paraffin.
- Kamara ng gas - matatagpuan sa itaas, na idinisenyo upang mangolekta ng mga gas mula sa reaksiyong kemikal.
- Gasket - matatagpuan sa itaas, gumaganap bilang isang sealant.
- Proteksyon na lalagyan - karton o lata upang maprotektahan laban sa kalawang at mga tagas ng electrolyte.
Isaalang-alang natin ang komposisyon ng isang saline battery mula sa isang kemikal na pananaw:
- Ang katod ay lubos na pinadalisay na zinc, lumalaban sa kalawang.
- Anode - pinaghalong MnO2, grapayt, pagpapabinhi ng electrolyte.
- Ang electrolyte ay ammonium chloride, o isang pinaghalong zinc chloride na may calcium chloride.
Aling mga baterya ang mas mainam: saline (1) o alkaline (2)?
Ang paghahambing ay maaaring gawin sa anyo ng isang talahanayan, kung saan ang mga kalamangan at kahinaan ng iba't ibang uri ng elemento ay malinaw na nakikita:
| Mga parameter ng paghahambing | 1 | 2 |
| Mga kondisyon ng temperatura, mga kondisyon ng pagpapatakbo | Nababawasan ang pagganap sa mababang temperatura at hindi makatiis sa mga pag-alon ng kuryente. | Gumagana nang maayos sa mababang temperatura - hanggang -20O, madaling makatiis ng mga surge, hindi natatakot sa isang matalim na pagtaas sa kasalukuyang load |
| Pinakamahusay bago ang petsa | 2-3 taon | 5 taon |
| Aplikasyon | Angkop gamitin sa mga device na may mababang konsumo ng kuryente | Angkop gamitin sa mga kagamitang may katamtaman at mataas na konsumo ng enerhiya |
| Mga instrumento, teknikal na aparato | Mga alarm clock, mga orasan sa dingding, mga remote control, maliliit na flashlight, mga simpleng laruan | Mga manlalaro, flashlight, laruang pangmusika, voice recorder, monitor ng presyon ng dugo |
Kapag pumipili ng pinagmumulan ng kuryente para sa isang aparato na may mga partikular na kinakailangan sa pagpapatakbo, mahalagang malaman kung paano makilala ang pagkakaiba sa pagitan ng saline battery at alkaline battery. Bagama't ang mga saline battery ay minarkahan ng letrang R, ang mga alkaline battery ay sinusundan ng letrang L (LR).
Mga konklusyon at rekomendasyon
Mas magaan at mas abot-kaya ang ganitong uri ng pinagmumulan ng kuryente. Gayunpaman, maikli ang shelf life ng mga saline batteries—2 hanggang 3 taon—at maaari silang sumailalim sa bahagyang self-discharge habang iniimbak, at habang ginagamit, kapag may biglaang pagtaas ng kuryente. Samakatuwid, dahil sa kanilang medyo mahinang pagganap ngunit medyo mababa ang halaga, madaling bumili ng ilang set ng baterya bilang backup.
Hindi matangkad kapasidadAng mga baterya ng asin (2-3 beses na mas mababa kaysa sa iba pang mga uri) ay nililimitahan ang kanilang paggamit sa mga simpleng aparato na may mababang kasalukuyang load.
Madaling matukoy kung posible bang mag-charge ng mga saline na baterya: ang pangalan ng baterya ay nakasaad sa katawan ng aparatong nilayon para sa pag-charge. kapasidadSa mAh. Kung hindi magagamit ang halagang ito, ito ay isang regular na baterya, at sa kabila ng maraming payo ng eksperto, hindi dapat ito i-charge. Ang pag-charge nito ay hindi magbibigay ng inaasahang pangmatagalang epekto at maaaring humantong sa isang aksidente dahil sa sobrang pag-init at pagtagas ng electrolyte. Kung kailangan mo ng mas maaasahan at pangmatagalang pinagmumulan ng kuryente, mas mainam na mamuhunan sa isang alkaline na alternatibo o isang rechargeable na baterya.
Kawili-wiling katotohanan: Baterya ng asin na gawa sa sarili Maaari itong gawin nang napakasimple. Kakailanganin mo ng 50-kopeck na barya, foil, papel, at solusyon ng asin. Pinakamainam na ibabad ang mga barya sa solusyon ng suka bago gamitin upang maalis ang anumang plaka o dumi. Buuin ang aparato: isang barya, papel na binabad sa solusyon ng asin, at foil. Ulitin ang prosesong ito nang ilang beses, na lumilikha ng isang haligi kung saan ang barya (positibo) ay nasa isang dulo at ang foil (negatibo) ay nasa kabila. Ang kuryente ay nalilikha ng potensyal na pagkakaiba na nilikha ng electrolyte (solusyon ng asin) sa pagitan ng metal ng foil at ng barya. Ang imbensyong ito ay tinatawag na voltaic pile, at ang boltahe nito ay direktang nakadepende sa bilang ng mga barya na ginamit: mas maraming barya, mas mataas ang boltahe na makukuha. Gayunpaman, pagkatapos ng eksperimento, ang mga barya ay hindi na magagamit; magkakaroon sila ng kalawangin na patong.